A kristályok növekedése
A növekedés laponként (rétegenként) történik (51. ábra).
Növekedési sebesség: a kristálylapoknak a felületre merőleges irányban történő eltolódásának sebessége
A növekedési sebesség a kristálytanilag különböző irányokban különböző, de egymással párhuzamos irányokban egyenlő.
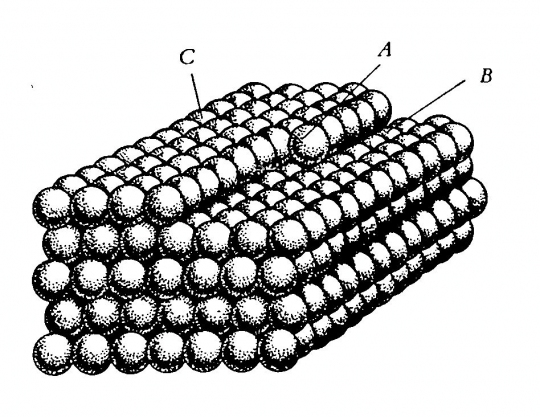 51. ábra. Egy kristálylap kialakulása.
51. ábra. Egy kristálylap kialakulása.
A következő atom főként az A betűvel jelölt helyre törekszik; a C és a B, helyzete kevésbé "vonzó"
A kristályok alakját a lapnormálisok (52. ábra) irányában mért növekedési sebességek aránya határozza meg (53. ábra).
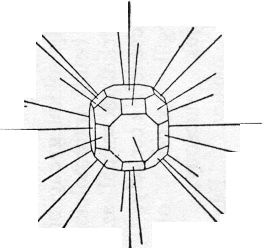 52. ábra. Egy kristály lapnormálisai
52. ábra. Egy kristály lapnormálisai
A kristályok méretét a gócképződés és gócnövekedés sebességének viszonya határozza meg.
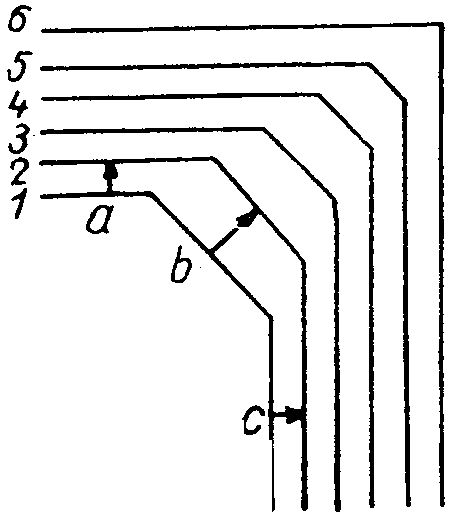 53. ábra. A kristályalak kialakulása. A gyorsabban növekvő b lap fokozatosan kisebbedik, majd teljesen eltűnik.
53. ábra. A kristályalak kialakulása. A gyorsabban növekvő b lap fokozatosan kisebbedik, majd teljesen eltűnik.
A kristályok növekedését befolyásoló tényezők
a., környezet hatása (bennőtt; fennőtt; ránőtt)
b., koncentráció (54. ábra).
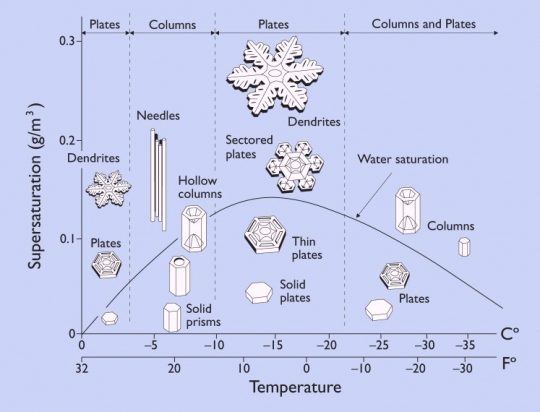 54. ábra. Az úgynevezett vázkristályok. A hópelyhek olyan közegben jönnek létre, amelyben a víz koncentrációja kicsi, a kristályosodás sebessége pedig nagy. Nincs idő az energiailag legkedvezőbb hely elfoglalására, ezért alakulnak ki vázkristályok.
54. ábra. Az úgynevezett vázkristályok. A hópelyhek olyan közegben jönnek létre, amelyben a víz koncentrációja kicsi, a kristályosodás sebessége pedig nagy. Nincs idő az energiailag legkedvezőbb hely elfoglalására, ezért alakulnak ki vázkristályok.
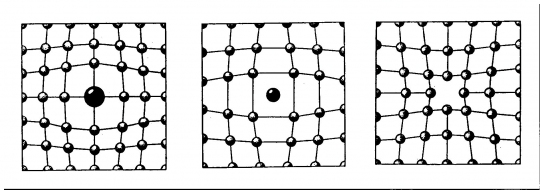
c., szennyezések (55., 56. ábra).
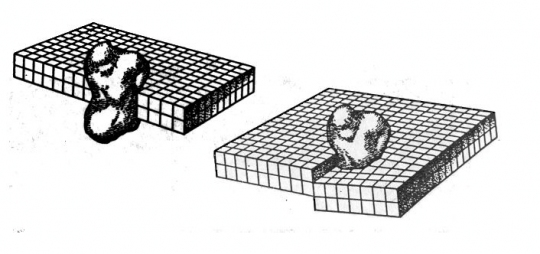 56. ábra. Egy porszem a kristályrácsban.
56. ábra. Egy porszem a kristályrácsban.
(A méretarányok valósághűek.)
A kristályok szabályszerű összenövései (57. ábra)
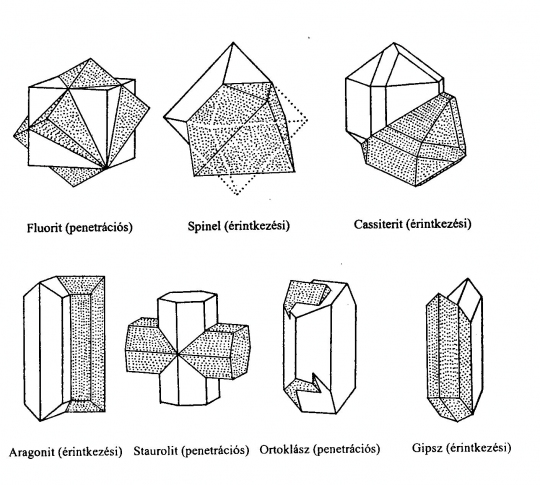 57. ábra. Példák az iker összenövésre
57. ábra. Példák az iker összenövésre
1., Azonos összetétel esetén:
Megkülönböztetünk szimmetrikus (iker) és párhuzamos (az orientáció azonos) összenövést; valamint egyszerű (2 egyed) és többszörös (nagyszámú egyed) összenövést.
Egyszerű összenövés esetén:
a., érintkezési (juxtapoziciós) ikrek (pl.: gipsz; spinell)
b., átnövéses (panetrációs) ikrek (pl.: pirit) (57. ábra
2., Különböző összetétel esetén:
Epitaxis (pl.: CaCO3- NaNO3)
Izotípia
Azokat a kristályokat amelyek hasonló külső alakot és hasonló belső felépítettséget mutatnak, izotip kristályoknak nevezzük (pl.: NaCl, KCl, PbS).
Izomorfia
Azokat az izotip kristályokat, amelyekben az ionok egymást helyettesíthetik (elegykristályokat alkothatnak) izomorfoknak nevezzük. (4.táblázat).
Feltételei:
a., közel azonos méretű tömegpontok,
b., közel azonos polarizációs sajátság,
c., azonos típusú és méretű elemi cella pl.: (CaCO3; NaNO3).
| KALCIT TÍPUS | ARAGONIT TÍPUS | ||||
| Ásvány | Képlete | Kation rádiusz (nm) | Ásvány | Képlete | Kation rádiusz (nm) |
| kalcit (mészpát) | CaCO3 | 0,106 | aragonit | CaCO3 | 0,106 |
| rodokrozit (málnapát) | MnCO3 | 0,091 | stroncianit | SrCO3 | 0,127 |
| smithsonit (cinkpát) | ZnCO3 | 0,083 | cerrusit | PbCO3 | 0,132 |
| sziderit (vaspát) | FeCO3 | 0,082 | witherit | BaCO3 | 0,143 |
| kobaltit | CoCO3 | 0,082 | |||
| magnezit | MgCO3 | 0,078 |
4. táblázat. Példák az izomorf sorokra
Az izomorf vegyületek atomjait, ionjait diadochnak nevezzük, ha viszonylagos nagyságuk és polarizálhatóságuk bizonyos határokon belül egyenlő. A diadoch elemek egymást bizonyos vegyületekben korlátlanul helyettesíthetik. Tökéletesen diadoch a Nb és a Ta [pl.: (Fe,Mn)(Nb,Ta)2O2].
Ha a helyettesítés nem csak egyes alkotókra, hanem a kristály egészére vonatkozik, elegykristályokról beszélünk. 15%-nál kisebb méretkülönbség esetén hézag nélküli, míg ennél nagyobb méretkülönbség esetén (a polarizációs sajátságok változatlan azonossága mellett) hézagos elegykristály-képződésről beszélünk.
Polimorfia (többalakuság):
Az azonos összetételű anyagoknak az a tulajdonsága, hogy különböző termodinamikai feltételek mellett különböző rácsszerkezetben jelennek meg. Elemek esetében allotrópiának nevezzük.
Átalakulás iránya: instabil ® stabil.
Átalakulási pont: az a hőmérséklet, amelyen az átalakulás megtörténik.
Átalakulási sebesség: lassú vagy gyors.
Átalakulás módja: enantiotrop vagy monotrop
1., Enantiotrop: (reverzibilis)
Az egyes módosulatok egy bizonyos hőmérsékleten, ugrásszerűen, a külső alak megváltoztatása nélkül felveszik a másik módosulat kristályrácsszerkezetét.
pl.: α-Fe ¬ 906°C λ-Fe
rombos-S ¬ 96,3°C ® monoklin-S
2., Monotrop (irreverzibilis)
A kristályrács nagyfokú megváltozásával jár, az átalakulás lassú.
pl.: aragonit 400°C ® kalcit
gyémánt 2000°C ® grafit
Pszeudomorfia (álalakúság):
Egy jellegzetesen kristályosodó ásvány kémiai összetétele, kémiai átalakulás következtében fokozatosan megváltozik, az új vegyület azonban "kölcsönveszi" az eredeti kristály alakját.
Pszeudomorfiát létrehozó kémiai átalakulások:
1. Anyagleadás: kuprit (Cu2O) ® réz (Cu)
2. Anyagfelvétel: malachit (Cu2 (OH)2 CO3) ® azurit (Cu3 (CO3)2 (OH)2)
3. Anyagcsere: pirit (FeS2) ® limonit (Fe2O3 . nH2O)
4. Teljes anyagcsere: kvarc (SiO2) ® fluorit (CaF2)